1 实验目的
(1)用电泳法测定氢氧化铁溶胶的ζ电势。 (2)掌握电泳法测定ζ电势的原理和技术。 (3)学习Fe(OH)3溶胶的制备和纯化。 (4)理解电泳是胶体中液相和固相在外电场作用下相对移动而产生的电性现象。
2 实验原理
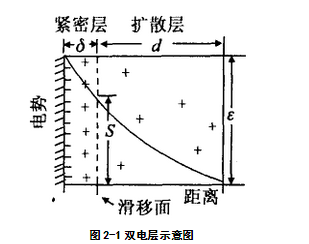
溶胶是一个多相体系,其分散相胶粒的大小约在1nm~1μm之间.校核大多是分子或原子的聚集体,因选择性地吸附介质中的某种离子(或自身电离)而带电。介质中存在的与吸附离子电荷相反的离子称为反离子,反离子中有一部分因静电引力(或范德华力)的作用,与吸附离子一起紧密地吸附于胶核表面,形成紧密层。于是,胶核、吸附离子和部分反离子(即紧密层)构成了胶粒。反离子的另一部分由于热扩散分布于介质中,故称为扩散层,见图2-1。
紧密层与扩散层间交界处称为滑移面(或Stern面)。显然紧密层与介质内部之间存在电势差,称为ζ电势。此电势只有处于电场中才显示出来。在电场中胶粒会向异号电极移动,称为电泳。在特定的电场中,ζ电势的大小决定于胶粒的运动速度,故ζ电势又称电动电势。
因为溶胶是高分散的多相的热力学不稳定体系。为了降低体系的表面能,它终将聚集而沉降,但它在一定条件下又能相对地稳定存在,主要原因之一是体系中胶粒带的是同一种电荷,彼此相斥而不致聚集。胶粒带的电荷越多,ζ电势越大,胶体体系越稳定。因此ζ电势大小是衡量溶胶稳定性的重要参数。
利用电泳现象可测定ζ电势。电泳法又分宏观法和微观法,前者是将溶胶置于电场中,观察溶胶与另一不含溶胶的导电液(辅助液)间所形成的界面的移动速率;后者是直接观测单个胶粒在电场中的泳动速率。对高分散或过浓的溶胶采用宏观法;对颜色太浅或浓度过稀的溶胶采用微观法。
本实验是在一定的外加电场强度下,通过测定Fe(OH)3胶粒的电泳速度然后计算出ζ电位。

式中:η, ε是测量温度下介质的粘度(Pa·s)和介电常数,取文献值;u为胶粒电泳的相对移动速率(m·s-1);(U/l)为电位梯度(V·m-1),U为两极间电位差(V),l为两极间距离(m);K是与胶粒形状有关的常数,球形粒子为6,棒状粒子为4,对于Fe(OH)3K值为4。
本实验中,测定电泳测定管中胶体溶液界面在t(s)内移动的距离d(m),求得电泳速度u=d/t。
Fe(OH)3溶胶用水凝聚法制备,制备过程中所涉及的化学反应如下: ①

