聚丙烯酰胺凝胶制备
4.1 清洗玻璃板、灌胶用量筒和烧杯,玻璃板气干(制胶用玻璃板为硫化玻璃,灌胶面必须干净无水分,否则灌胶时容易产生气泡;烧杯、量筒和玻璃板如果有水,由于胶与水不相溶,易使胶不能牢固粘在玻璃板上);
4.2将平口玻璃板和凹口玻璃板放在桌面的支撑物(瓶盖等)上,给玻璃板滴少量100%乙醇,用质量好的纸均匀擦洗制胶面,气干;
4.3 平口玻璃板和凹口玻璃板的三个边均匀的涂抹适量凡士林(凡士林太多不容易清洗);放上需要厚度的板条,此步应注意密封好板条的相接处,用手将三边和接茬处按牢固,否则容易漏胶;然后用夹子(夹子夹在板条中间)将玻璃板固定于灌胶架上;
4.4 配胶(8%非变性聚丙烯酰胺凝胶,Acr:Bis=37.5:1)、灌胶;
将以下母液按量混合均匀保存于4℃,一般一周内用完,
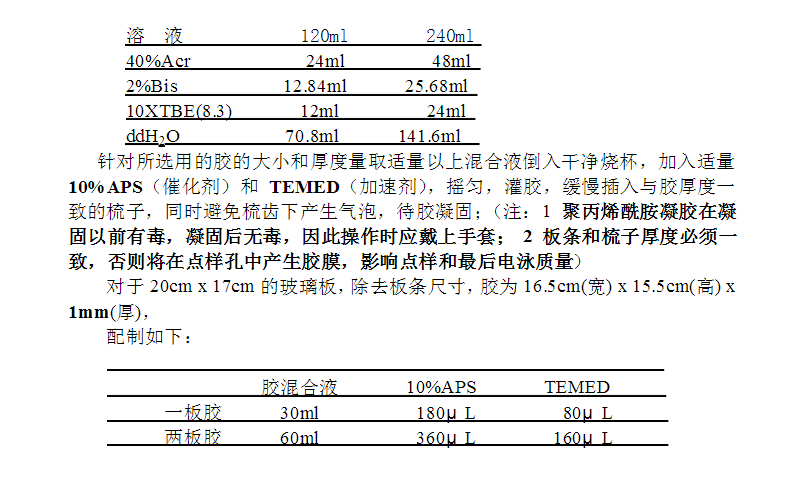
制胶及电泳
(1)胶板的准备:首先确定两块玻璃板是否平整,用去污剂和清水将玻璃板洗涤干净,并用蒸馏水冲洗,晾干后用95%乙醇擦拭。
1 用1~2 ml 95%的乙醇依次将长玻璃和短玻璃的正面擦拭干净、均匀;(以平整、光滑的一面为正面)(**次用的玻璃板**好擦2~3次)
2 用加样枪取1ml配置好的亲和硅烷均匀分布于长玻璃的正面,用纱布涂抹均匀;(**次用的玻璃板**好用亲和硅烷擦2~3次)
3 用加样枪取0.5~1ml配置好的剥离硅烷均匀分布于长玻璃的正面,用纱布涂抹均匀;(擦**感觉特别光滑为止)
4 用1ml 95%的乙醇依次将长玻璃和短玻璃的正面擦拭均匀;(可使亲和硅烷和剥离硅烷分布更未均匀,也可擦去多余部分)
5 检查玻璃板正面有误纱布绒毛之类的异物,若有,可吹走;取0.4mm的边条,用纱布擦净,置于长玻璃板的左右两侧,靠边放置,将短玻璃板压于长玻璃板上,调整边条和短玻璃板的位置,使边条刚好处于边缘位置,但不突出,且长短玻璃板刚好对其,用夹子固定住玻璃板的两侧;以1×TAE配制1%琼脂糖凝胶并封住玻璃板底部,待凝胶凝固后用医用胶带密封;将玻璃板凹槽向上小角度倾斜放置,准备灌胶。
(2)制胶:称取尿素21g,加入17ml双蒸水加热约二三十秒溶解,待冷却后加入10ml 5×TBE,冰浴**冰手时加入7.5ml 40%丙烯酰胺(19:1),然后加入225μl 10%过硫酸铵和50μl TEMED,快速混匀,准备灌胶。
(3)灌胶:用5ml加样枪将制备好的胶液沿玻璃板中部缓慢加入到胶板玻璃板之间的空隙,注意不能在胶中形成气泡(要多次实验以掌握技巧、控制加样速度、调节玻璃板倾斜度、手按、竖起玻璃板、便轻敲变加样等)。胶灌满后,将鲨鱼齿的平端插入胶液下5mm左右(不可过深,以免后面不能加样;也不可过浅,以免上样量过小),同时防止梳齿平端下方出现气泡,于室温下静置2h,使胶完全聚合后使用。
(4)预电泳:撕去胶布,两端平行用力拔出梳齿,将玻璃板和梳齿上的多余凝胶擦洗干净,用蒸馏水漂洗玻璃板、梳子。将玻璃板装到
电泳槽上,在下方
电泳槽中加入1×TBE**没过玻璃板下端约1cm,装好
电泳槽,加入1×TBE**没过玻璃板上端约1.5cm处,用梳齿刮去玻璃板间隙间的碎胶,再用5ml加样枪将其吹干净,反转梳齿,将鲨鱼齿插入凝胶胶面下约0.5mm,并用夹子夹紧,梳齿间空隙即为加样孔。120w恒功率,预电泳30min。
(5)点样:点样前用加样枪吹吸每个上样槽,将梳齿间隙间油状液体吸干净,以利于样品更好的沉降。把DNA样品与上样缓冲液混合,每个加样孔加5~7μl的扩增产物。
(6)电泳:140-160w恒功率电泳,待溴酚蓝**胶的四分之三处时(大约需要1.5~2h),终止电泳,回收电泳液(可重复用一段时间,当发现电压下降很多时要更换电泳液,或者补加蒸馏水可继续用一段时间),取下胶板,将两块玻璃板轻轻分开,凝胶留在长玻璃板上。 银染显色
6.1 当**染料接近胶底边缘,电泳结束,也可使**染料跑出;关闭
电泳仪,
移去夹子,取下玻璃板,将胶从玻璃板上小心取下,切去一角或两个角作为记号,以便于辨认,然后开始银染处理,处理均在摇床上进行,具体步骤如下:
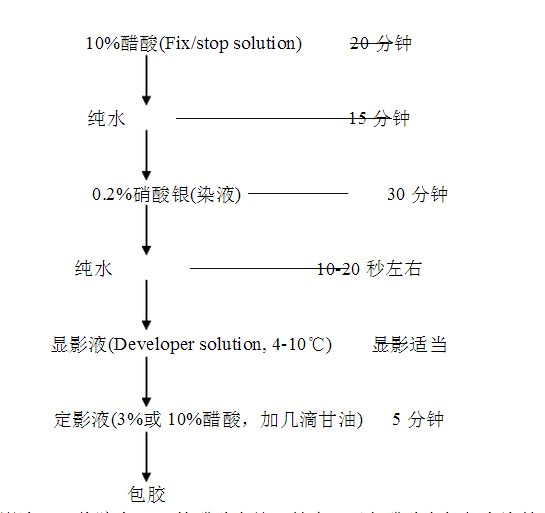
注:定影液——将胶在10%的醋酸中处理结束,可向醋酸中加入少许甘油(防止胶在干燥过程中发生胶裂),摇匀,直接用作定影液;
银染中应注意事项:
① 水的质量对染色效果影响极大,一般用超纯水或双蒸水,如果水含有污染物,胶可能不显影或仅仅显上部条带;而下部空白;
② 显影液中碳酸钠的纯度也很重要,建议使用无水碳酸钠;
③ 由于温度过高,显影太快,所以为了便于控制显影过程,一般将显影液储存
于4℃,用时取出;显影液在4℃长期放置容易结晶,一般使用前1-2天配制即可,显影液配制方法如下:
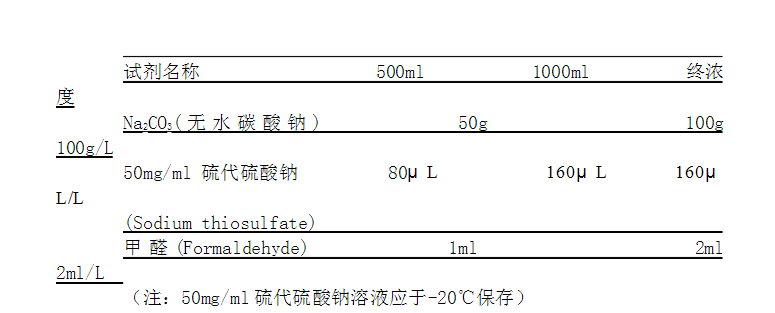
#p#分页标题#e#
④ 在10%的定影液加入几滴甘油,可以用作**后的显影液; ⑤ 每一步都应该轻微摇动,一般在摇床上进行;
⑥ 银染后在无离子水中的冲洗时间要求十分严格,一般在10秒左右,应小于20秒,如果超过20秒,应重新在0.2%的硝酸银重新染30分钟;
⑦ 0.2%的硝酸银溶液可以重复使用6-7次,每次适当延长银染时间,**后可以在废弃银液中加入NaCl,使银以AgCl2沉淀,过滤或重力沉淀即可以回收银; ⑧因为不容易清洗,所以装硝酸银、显影液和固定液及定影液的盆不能混用; ⑨电泳结束后,涂抹凡士林的玻璃板、板条用热水浸泡后,用纸擦去凡士林,再清洗时比较容易洗净,或浸泡后用洗洁精清洗即可。 7 包胶
将包胶用的玻璃板洗净,玻璃纸提前泡在水中30-60分钟。包胶时,先在玻璃板上铺一张玻璃纸,赶净气泡,四边向下抹平;将胶放在玻璃纸上,再用另一张玻璃纸盖在胶上,赶净气泡,四边向下抹平,将玻璃板放在吸水纸上,在室温(25℃)或恒温箱中干燥(由于恒温箱透气性差,干燥过程慢),干燥好的胶可以用热钢锯条封四边;照相或干胶扫描。


 #p#分页标题#e#
#p#分页标题#e#